Emil Fischer
| Họ và tên | Hermann Emil Fischer |
| Ngày sinh | 9/10/1852 |
| Ngày mất | 15/7/1919 |
| Quốc tịch | Đức |
| Lĩnh vực chuyên môn | Hoá học |
| Giải thưởng đã đạt được | Huân chương Davy (1890) Hội viên Học viện Khoa học Hoàng gia Anh (1899) Giải Nobel Hóa học (1902) Giải thưởng Giảng bài Faraday (1907) Huân chương Elliott Cresson (1913) |
Hermann Emil Fischer sinh ngày 9 tháng 10 năm 1852 tại Euskirchen, Đức trong gia đình có người cha là một thương nhân thành đạt. Ngay từ nhỏ, ông đã luôn là một học sinh với thành tích học tập xuất sắc và có đam mê mãnh liệt với vật lý, nhưng cha lại muốn ông kế nghiệp công việc kinh doanh của gia đình. Vì vậy, sau một thời gian thử việc bất thành, Emil được cha gửi đến Đại học Bonn vào năm 1871 để học hóa học. Tại đây, ông tham dự các bài giảng của Kekulé, Engelbach và Zincke, đồng thời theo học lớp vật lý của August Kundt và khoáng vật học của Paul Groth.
Tuy nhiên, vào năm 1872, Emil được anh họ thuyết phục cùng đến Đại học Strasbourg mới thành lập – nơi Giáo sư Rose đang nghiên cứu phương pháp phân tích Bunsen. Tại đây, ông đã gặp Adolf von Baeyer – người có tác động mạnh mẽ nhất đến quyết định đi theo con đường hoá học của ông. Dưới sự hướng dẫn của von Baeyer, Emil nghiên cứu về thuốc nhuộm phthalein và vào năm 1874, ông lấy bằng tiến sĩ tại Strasbourg với luận văn về fluoresceine và orcin-phthalein. Cùng năm đó, ông được bổ nhiệm làm trợ giảng tại Đại học Strasbourg và tại đây ông đã phát hiện ra bazơ hydrazine, phenylhydrazine và chứng minh mối quan hệ của nó với hydrazobenzene và một axit sunfonic. Phát hiện này có liên quan đến rất nhiều công trình sau này của Emil.
NHỮNG ĐÓNG GÓP TO LỚN CHO HOÁ HỌC
Năm 1874, Fischer trở thành trợ lý riêng trong phòng thí nghiệm nghiên cứu của Baeyer nhưng ông đã rời đi vào năm 1881 để thành lập phòng thí nghiệm của riêng mình. Sau đó, ông bắt đầu áp dụng các phương pháp hóa học cổ điển của hóa học hữu cơ để xác định cấu trúc của các hợp chất sinh học như đường, purin và protein.
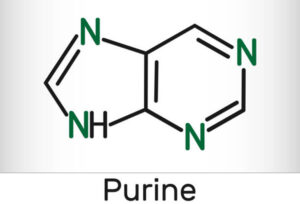
Nghiên cứu về Purin và Đường
Cấu tạo của Purin (Nguồn: IHR Vietnam)
Fischer nghiên cứu về purin từ năm 1882 đến năm 1906. Trong khoảng thời gian này, ông đã chứng minh rằng axit uric, xanthine, caffeine và các hợp chất tự nhiên khác đều thuộc về một họ đồng nhất. Chúng có thể có nguồn gốc từ nhau và tương ứng với các dẫn xuất hydroxyl và amino khác nhau của cùng một hệ thống cơ bản được hình thành bởi cấu trúc nitơ hai vòng mà nhóm urê đặc trưng tham gia vào. Chất này được ông gọi là purin, và ông đã tự tổng hợp nó vào năm 1898. Nhiều dẫn xuất nhân tạo có phần tương đồng với các chất xuất hiện trong tự nhiên, cũng đã được điều chế từ phòng thí nghiệm của ông trong khoảng thời gian từ 1882 đến 1896.
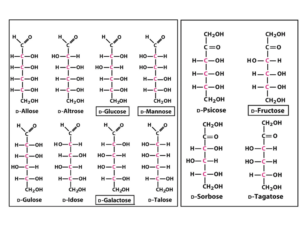
(Nguồn: Cheng)
Năm 1884, Fischer bắt đầu một nghiên cứu dài hạn để xác định cấu trúc hóa học và cấu hình không gian của các đồng phân đường glucose, galactose, fructose và sorbose – với mục đích xác định nguồn gốc của sự đồng phân của chúng. Chìa khóa của nghiên cứu này là phản ứng của đường với phenylhydrazine. Bản thân các loại đường rất khó tinh chế và xác định đặc tính, nhưng chúng phản ứng với phenylhydrazine (hợp chất hữu cơ thường được sử dụng trong tổng hợp indole) tạo ra osazone, là các hợp chất tinh thể cao, dễ tinh khiết. Fischer nhanh chóng nhận ra rằng những loại đường này là đồng phân không gian và có thể được phân biệt bằng cách áp dụng lý thuyết về về nguyên tử cacbon bất đối xứng của Van’t Hoff và Le Bel. Fischer nhận ra rằng các đồng phân glucose đã biết chỉ đại diện cho 4 trong số 16 đồng phân không gian có thể có theo lý thuyết của van’t Hoff. Bằng cách sử dụng các dẫn xuất osazone và kỹ thuật tổng hợp đường do các nhà hóa học Đức Bernhard Tollens và Heinrich Kiliani phát triển, Fischer không chỉ có thể phân biệt các đồng phân đã biết mà còn tổng hợp được chín đồng phân dự đoán. Năm 1890, ông đã tổng hợp được glucose, fructose và mannose từ glycerol. Đây là thành công lớn nhất trong quá trình nghiên cứu về đường của ông.
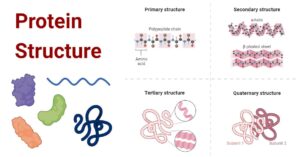
Nghiên cứu Enzyme và Protein
Cấu trúc của protein (Nguồn: Microbe Notes)
Năm 1892, Fischer được chọn làm giáo sư hóa học tại Đại học Berlin, lúc bấy giờ là viện hóa học lớn nhất và uy tín nhất ở Đức. Dưới sự lãnh đạo của ông, viện hóa học ở Berlin trở thành một trong những nơi sôi động nhất cho tất cả các lĩnh vực hóa học trên thế giới. Ông đã hướng dẫn nghiên cứu của hàng trăm học sinh và cộng sự từ Châu u, Bắc Mỹ và Nhật Bản.
Tại Berlin, nghiên cứu của Fischer chuyển sang lĩnh vực enzyme và protein. Nghiên cứu sâu rộng của Fischer về đường bao gồm việc điều tra tiêu hóa đường của chúng bằng men bia, và ông phát hiện ra rằng trong số các đồng phân lập thể glucose t, chỉ một số ít có khả năng bị tiêu hóa bởi các enzyme trong men bia. Bởi vì những đồng phân này chỉ khác nhau về đặc tính không gian, Fischer kết luận rằng enzyme trong men bia cũng phải có một định hướng không gian cụ thể để tiếp nhận phân tử đường và phản ứng với nó.
Ngoài ra, Fischer cũng tham gia vào việc thiết lập cấu trúc hóa học của enzyme và protein. Protein vốn được biết đến là cấu tạo từ các axit amin, nhưng Fischer đặc biệt đề xuất rằng các axit amin trong protein được liên kết với nhau bằng liên kết amid. Fischer gọi đây là liên kết peptid. Ông đã xác định sự hiện diện của lớp phân tử này trong protein bằng cách phát triển các phương pháp tổng hợp để tạo ra chuỗi dài các axit amin được giữ lại với nhau bằng liên kết peptid để tạo thành các chất giống protein. Năm 1907, ông đã tạo ra một polypeptide với 18 axit amin và chứng minh rằng nó có thể bị phá vỡ bởi enzyme theo cách tương tự như một protein tự nhiên.
Ngoài công việc vĩ đại của mình trong các lĩnh vực đã được đề cập, Fischer còn nghiên cứu các chất hóa học trong địa y mà ông tìm thấy trong những kỳ nghỉ ở Rừng Đen, cũng như các chất được sử dụng trong nhuộm da và chất béo.
Thành tựu
Fischer được phong làm Cố vấn Cơ mật Phổ (Geheimrat) và nhận bằng danh dự Tiến sĩ từ các trường Đại học Christiania, Cambridge (Anh), Manchester và Brussels. Ông cũng được trao Huân chương Phúc lợi Phổ và Huân chương Maximilian vì Nghệ thuật và Khoa học. Năm 1902, ông nhận Giải Nobel Hóa học cho công trình nghiên cứu về đường và purin.
Trong thời gian ở Berlin, Fischer tích cực tham gia vào việc thúc đẩy hóa học và khoa học ở Đức. Ông đóng vai trò quan trọng trong việc thành lập Hội Kaiser Wilhelm và các viện nghiên cứu hóa học và vật lý liên quan vào năm 1911. Ông cũng tham gia tổ chức sản xuất hóa chất ở Đức trong Chiến tranh Thế giới I.
CUỘC SỐNG CÁ NHÂN VÀ NHỮNG NGÀY CUỐI ĐỜI
Huân chương Emil Fischer (nguồn: cgb.fr)
Trong khoảng thời gian sống tại Würzburg, ông tận hưởng những chuyến đi bộ giữa những ngọn đồi và thường xuyên đến thăm Rừng Đen. Ngoài ra, ông còn là một nhà vận động kiên trì trong việc thành lập các tổ chức khoa học, không chỉ trong lĩnh vực hóa học mà còn cả trong các lĩnh vực khác. Bên cạnh đó, Fischer là một người có trí nhớ tuyệt vời. Nhờ đó, ông vẫn có thể ghi nhớ các bản thảo bài giảng đã viết. Sự hiểu biết sâu sắc về các vấn đề khoa học, trực giác, lòng yêu sự thật và sự kiên trì chứng minh các giả thuyết bằng thực nghiệm đã đánh dấu ông là một trong những nhà khoa học vĩ đại nhất mọi thời đại.
Năm 1888, Fischer kết hôn với Agnes Gerlach. Không may, vợ ông qua đời sau bảy năm kết hôn. Họ có ba người con trai. Người con trai thứ ba, Hermann Otto Laurenz Fischer, là Giáo sư Hóa sinh tại Đại học California, Berkeley.
Emil Fischer qua đời năm 1919. Để ghi nhận những đóng góp to lớn trong sự nghiệp của ông, Hiệp hội Hóa học Đức đã thành lập giải thưởng Huân chương Emil Fischer.
TÀI LIỆU THAM KHẢO